Huvudskillnad: Absorption är ett massfenomen där en absorbering helt penetrerar i kroppen av en fast eller flytande för att bilda en förening eller en lösning. Å andra sidan är adsorption ett ytfenomen där molekyler av ett adsorbat endast koncentreras på ytan av ett adsorbent.
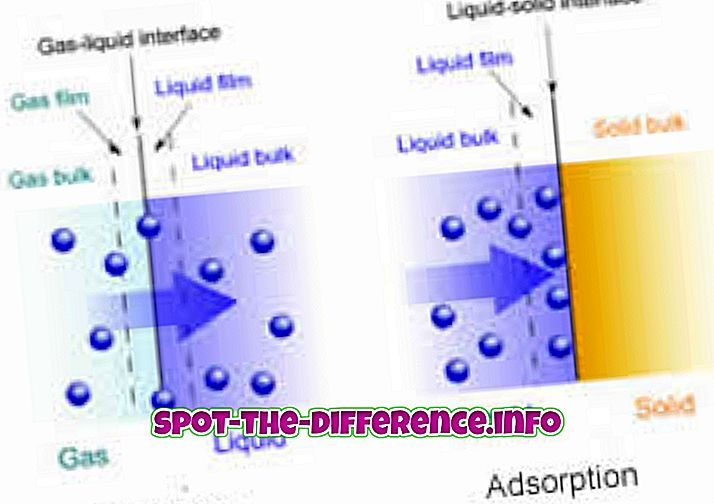
Kemisk reaktion - koldioxid absorberad av en lösning av kaliumkolväte
Fysisk process - Luft absorberas i vatten genom att lösa upp

Det finns två typer av adsorptionslägen - kemiska och fysiska. Vid kemisk adsorption är molekylerna och ytan bundna av svaga Vander Walls styrkor. Å andra sidan bildas kemisk bindning mellan molekyler och yta vid kemisk adsorption.
Därför är den primära skillnaden mellan adsorption och absorption att absorption är ett massfenomen vilket innebär att det händer genom materialets kropp, medan adsorption förblir en ytfenomen. Adsorptionen är alltid exoterm, medan absorptionen är endoterm. Sorption innefattar både absorptionsprocesser och adsorption.
Jämförelse mellan adsorption och absorption:
Adsorption | Absorption | |
defintion | Uppsamling av ett gas- eller vätskebaserat ämne på ytan av ett fast ämne eller en vätska | Diffusion av ett ämne i en vätska eller fast substans för bildning av en lösning eller förening |
Exempel | Inerta gaser adsorberas på kol. | En torr svamp absorberar vatten |
Värmeväxling | Exoterm med undantag för adsorption av H2 på glas | Endotermisk |
Uppnå jämvikt | Jämförelsevis snabbare | Jämförelsevis långsamt |
Koncentration | Koncentrationen på adsorbentens yta är annorlunda än i volymen | Koncentrationen är densamma i hela materialet |
Förekomstfrekvens | Det är snabbt inledningsvis men senare börjar kursen minska | Den äger rum med en jämn takt |