Huvudskillnad: Molaritet, även känd som molär koncentration, mäter antalet moler av en substans närvarande i per liter lösning. Molaritet betecknas med en huvudstad M. Molality mäter antalet mol av en substans närvarande i kilo lösningsmedel. Molality betecknas med ett mindre fall m.
Båda koncepten baserar sina beräkningar på hur många mol är närvarande i den nuvarande lösningen. En lösning kan definieras som en homogen blandning, vilket innebär att två eller flera komponenter har blivit blandade till den punkt som det inte kan särskiljas med blotta ögat. Dessa två begrepp kräver förståelse av mol eftersom det bestämmer antalet mol närvarande i lösningen. Teorin om mol upptäcktes av italiensk forskare Amedeo Avogardo.
1811 föreslog Avogardo att volymen gas, vid en given temperatur och tryck, är proportionell mot antalet atomer eller molekyler oavsett dess natur. Detta koncept kallas Avogardo konstanten. Det definieras som antalet beståndsdelar (vanligtvis atomer eller molekyler) i en mol av en given substans. Enligt lekmen skulle en mol av ett ämne representera antalet atomer och molekyler närvarande i elementet. Till exempel: Syre har en atomvikt på 16, detta skulle representera massan per mol syre. Så, en mol syre skulle ha en massa av 16 gram. Enligt Avogardo skulle en mol syre ha samma antal atomer som en mol väte. De kan dock skilja sig åt i vikt.
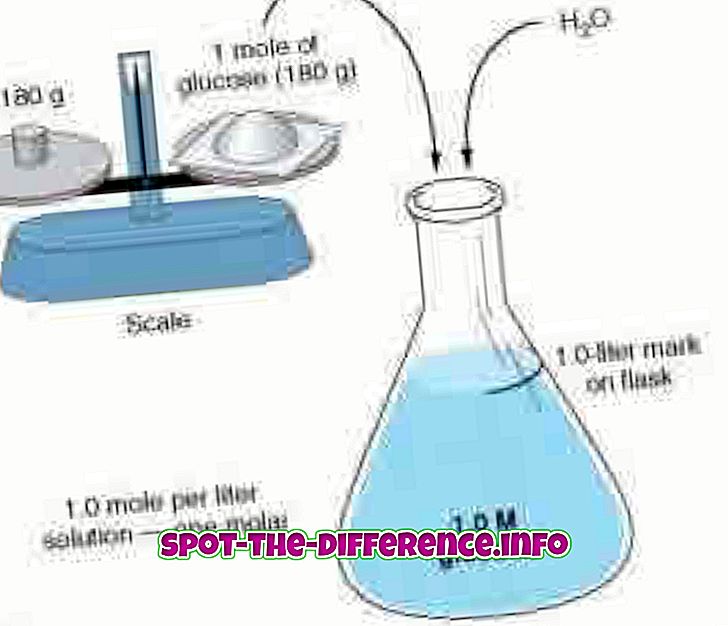
Molaritet och molalitet mäter koncentrationen med två olika metoder. Molaritet, även känd som molär koncentration, mäter antalet moler av ett ämne närvarande i per liter lösning. Molaritet betecknas med en huvudstad M. Således skulle en lösning med 1, 0 M ange att den innehåller 1 mol lösningsmedel per liter lösning. Till exempel: En lösning av vatten och socker. Om lösningen mäts som 1, 0 M, har lösningen 1 mol socker per liter lösning närvarande. Molaritet är också känd som koncentration av mängden substans, mängden koncentration, ämneskoncentration eller helt enkelt koncentration. Molariteten kan beräknas med formeln: M = mol (# mol) / L (volym lösning i liter).

Molality mäter antalet mol av ett ämne som finns i kilogram lösningsmedel. Molality betecknas med ett mindre fall m. Så en lösning med 1, 0m skulle ange att den innehåller 1 mol lösningsmedel per kilo lösningsmedel. Låt oss differentiera lösningen från lösningsmedel. Lös är substansen som upplöses i ett annat ämne. Ett lösningsmedel är ett ämne som löser upp lösningen. Så, om vatten och socker blandas ihop, skulle socker vara lösningsmedel och vatten lösningsmedlet. Blandat sockervatten skulle vara lösningen. Nu är det i molalitet av yttersta vikt att molerna delas av lösningsmedlets massa och inte lösningen. Molalitet kan beräknas med formeln: m = mol (# mol) / KG (massa av lösningsmedel i kg).
Varför skillnaden? Nåväl, båda används för att hantera temperaturen. Om en lösning kommer att förändras i temperaturen används molalitet. Men för lösningar som kommer att förbli vid konstant temperatur används molaritet. Detta beror på att när temperaturen stiger eller faller förändras volymen av lösningen och detta påverkar direkt molariteten. Därför används molalitet för att beräkna koncentrationen.